| المجلد 6 ,
العدد 5
, جمادى الأولى 1433 - نيسان (أبريل) 2012 |
| |
| دراسة التلوث الجرثومي والفطري لبعض الأشكال الصيدلانية الفموية المائية المصنّعة محلياً |
| Study of Bacterial and Fungal Contamination of Some Aqueous Oral Pharmaceutical forms Locally Manufactured |
| د. مصطفى العموري |
| Mustafa Al-Amori |
| كلية الصيدلة، جامعة دمشق، الجامعة الدولية الخاصة للعلوم والتكنولوجيا |
| الملخص Abstract |
تهدف هذه الدراسة إلى تقييم نجاعة حوافظ شرابات فموية مائية سورية غير عقيمة مختلفة. حيث مُيّزت جراثيم الُسْتَفْرَدات isolates السريرية تبعاً لخواصها الكيميائية الحيوية باستخدام طريقة معيارية لاستعرافها. وأُقحمت حوالي 105-107 خلية جرثومية معين هويتها لكل 1 مل من الشرابات المختبرة والتي حُضنت بعد ذلك لمدة 14 يوماً. قورن نمو الجراثيم ضمن الشراب بتعداد الجراثيم القادرة على الحياة من مزارع فرعية للشراب المقحم بالجراثيم في فترات زمنية مختلفة (0، 3، 6، 12، 24 ساعة، 3، 7، 14، 28 يوماً).
أظهرت المعطيات تراجعاً كبيراً في عدد الجراثيم القادرة على الحياة CFUs لكل من الجراثيم المستخدمة في الشرابات المختبرة كافة بعد أسبوع واحد من زمن الإقحام، حيث وصل عدد CFUs إلى الصفر في الشرابات كلها، عدا شراب مستعلق مضاد للحموضة استمر فيه عدد الجراثيم القادرة على الحياة بعد 14 يوم حضن حوالي 102 خلية لكل 1 مل من الشراب مع جميع الجراثيم االمستخدمة جميعها. وكشفت النتائج أن الفعالية المضادة للجراثيم لأنظمة الحفظ للشرابات المفحوصة جميعها كانت ممتازة وفقا ًلمواصفات دستور الأدوية الأمريكي USP.
|
| The study aims to evaluate the efficacy of preservatives of different non-sterile Syrian aqueous oral syrups. The clinical isolates microorganisms were characterized according to their biochemical properties by using standard method to their identification. The identified microorganisms were inoculated into tested syrups with 105-107 cfu/ml which were then incubated for 14 days. Growth of microorganisms into syrup was compared by counting the CFUs from a subculture of inoculated syrup at different time (0, 3, 6, 12, 24 hrs, 3, 7, 14 and 28 days).
The data exhibited great reduction of the CFUs count of each used microorganisms in all tested syrups after one week of incubation time , the count of CFUs was zero with all syrup, except anti-acid suspension which the count of CFUs maintained around 102 after 14 days of incubation time with all used microorganisms. The results revealed that the Antimicrobial effectiveness of preservation systems of all examined syrups were excellent according to the USP scales.
|
| المقدمة Introduction |
تتأثر ثباتية الأشكال الصيدلانية غير العقيمة بجملة من العوامل، من بينها المحتوى الجرثومي لتلك الأشكال، وكذلك قدرتها على مقاومة التلوث الجرثومي من خلال احتوائها على مواد حافظة بالإضافة إلى عوامل فيزيائية وكيميائية، ضمن الشكل الصيدلاني أو محيطة به (1). وفي الآونة الأخيرة تزايدت عمليات سحب المستحضرات الصيدلانية من الأسواق في مناطق مختلفة حول العالم. وعن أسباب ذلك بينت دراسة أجرتها رابطة الدواء والغذاء FDA عام 2005 أن 3% من المستحضرات المسحوبة سببها عدم الثبات من الناحية الجرثومية (6). ومن المعلوم أن الجراثيم قادرة على النمو في المنتجات الصيدلانية لما تحويه هذه المنتجات من مواد غذائية، وهذا النمو يجعل المنتجات غير آمنة وغير مقبولة للاستخدام (1).
فلقد سُحبت العديد من الأشكال الصيدلانية الفموية بسبب التلوث الجرثومي في الولايات المتحدة الأمريكية مثل المستعلقات المضادة للحموضة، وشرابات السعال (6). ولقد لوحظ أيضاً انتقال العدوى بجراثيم خطرة ( Enterobacter وK.pneumoniae وE.coli وSerratia) نتيجة استخدام مراهم وغسولات اليد، كما أكدت دراسات عدة أن المسكرة كانت السبب في نقل العدوى للعين (7)، وكذلك انتقال الزائفة الزنجارية بوساطة مرهم ستيرويدي (7). لذلك من الشائع إضافة المواد الحافظة إلى الأشكال الصيدلانية غير العقيمة (شرابات، كريمات، مواد تجميل، ........الخ ) وإلى الأشكال العقيمة غير الحقنية (الأشكال الصيدلانية العينية) والأشكال الحقنية متعددة الجرعة وذات الحجم الصغير (لا يتجاوز 30 مل) (8). المواد الحافظة هي مواد كيميائية قادرة على إنقاص عدد الجراثيم أو منعها من النمو، عند وجودها في المستحضر الصيدلاني، لذلك فإن المادة الحافظة الجيدة هي التي لها قدرة على القضاء على التلوث الجرثومي بسرعة وأثارها الجانبية قليلة جداً، وهي آمنة وثابته ضمن المستحضر الصيدلاني طيلة مدة الحفظ ومتوافقة مع مجمل مكونات الشكل الصيدلاني (2). غير أن هنالك مجموعة من العوامل التي تؤثر على فاعلية المادة الحافظة، مثل درجة حرارة حفظ الشكل الصيدلاني، حيث تزداد فاعلية المادة الحافظة بزيادة درجة الحرارة (5، 10). ولدرجة حموضة pH الشكل الصيدلاني أيضا تأثير، حيث أن المستويات الحمضية تعد ملائمة لفاعلية المواد الحافظة التي هي بمثابة حموض ضعيفة (10)؛ وكذلك فإن لنسبة الرطوبة (فاعلية الماء water activity Wa) ضمن المستحضر الصيدلاني دور في ثباته، حيث أن خفض قيمة فاعلية الماء يؤدي إلى تثبيط النمو الجرثومي (9). ولكي يبقى الشكل الصيدلاني ثابتاً خلال مدة الخزن والاستعمال، ينبغي على المصنّع أن يأخذ بعين الاعتبار شكل العبوة، الذي يساعد في التقليل من التلوث خلال استعمال المستحضر (7).
يهدف واضعو صيغة الدواء جميعهم إلى خفض تركيز المادة الحافظة ضمن المستحضر الصيدلاني لما لها من تأثيرات جانبية على الشكل الصيدلاني وعلى المستهلك؛ مع الحفاظ على فاعلية حفظ جيدة. ويجري ذلك من خلال التعويل على عامل أخر يساعد في حفظ المستحضر الصيدلاني، بالإضافة إلى المادة الحافظة (مثل الـ pH، وفاعلية الماء Wa، وحرارة الحفظ، ووجود مواد كيميائية ضمن الشكل الصيدلاني ...الخ)، لذلك نشأ تعبير نظام الحفظ Preservative system. وللتأكد من قدرة نظام الحفظ على حماية الشكل الصيدلاني خلال مدة التخزين والاستعمال، وجدت اختبارات ما يعرف بقدرة الحفظ Preservative capacity ، والتي تعتمد في مبدئها على إقحام كمية من أحد الجراثيم ضمن الشكل الصيدلاني ثم مراقبة ما سيحدث على الشكل الصيدلاني من تبدلات خلال مدة من الزمن حددتها دساتير الأدوية (9).
تهدف دراستنا إلى اختبار قدرة الحفظ في مجموعة من الأشكال الصيدلانية السائلة (شرابات، مستعلقات) من السوق السورية، ولشركات دوائية محلية مختلفة، وباستخدام جراثيم معزولة سريرياً أو من المحيط.
|
| المواد والطرق |
أُخذت، بشكل عشوائي، مجموعة من الأشكال الصيدلانية الفموية السائلة (عدا المضادات الحيوية) المطروحة في الصيدليات في سورية والمصنّعة محلياً، حيث استخدمت خمس عبوات من كل من:
أ- شراب مستعلق A وB؛
ب- شراب سائل C، D، E، F، G، H، I، J.
جرى اختبار قدرة الحفظ للعينات السابقة باستخدام ذرارٍ جرثومية معزولة من عينات سريرية (جرى تشخيصها وتعيين هويتها وحساسيتها للمضادات الحيوية بالطرق المرجعية) وهي: الإشريكية القولونية E. coli، واالعنقوديات الذهبية S. aureus، والكلِبْسيلَّة الرئوية K. pneumoniae، والزائفة الزنجارية P.aerugenosa.
واستخدم فطر المبيضات البيض Candida albicans المعزول من عينات سريرية، أما فطر الرشاشيات السوداء Aspergillus niger فجرى عزله من البيئة (جرت عملية تشخيص وتعيين هوية الفطور المستخدمة بالطرق المرجعية).
يُنجز اختبار قدرة الحفظAntimicrobial effectiveness test أو اختبار التحدي Challenge test بزرع الشكل الصيدلاني بحوالي 105-107 خلية جرثومية لكل 1 مل من المنتج حسب دستور الأدوية الأمريكي 30 (9). ثم حضن الأشكال الصيدلانية جميعاً بدرجة حرارة 22.5±2.5°م (درجة حرارة الصيدلية). بعد ذلك أخذت العينات بالفترات الزمنية التالية: 0-3-6-12-24 ساعة، ثم 3، 7 أيام، 14، 28 يوماً.
زرعت العينات الجرثومية على سطح وسطTrypticasein Soya Agar (TSA) ، في حين زرعت العينات الفطرية على وسط Sabouraud Dextrose Agar (SDA) (من شركة Conda، ايطاليا) بطريقة الفرش على السطح، علماً أنه جرت عملية مراقبة مصدوقية هذه الطريقة من خلال حساب معدل الاسترداد Recovery rate والذي كان 75% للأشكال الصيدلانية جميعها (9). تؤخذ العينة من الشكل الصيدلاني ومن ثم تجرى لها سلسلة تمديدات عشرية مناسبة بسائل تمديد مؤلف من مصل فيزيولوجي مع توين 20 بنسبة 3% (كمادة مبطلة لفاعلية المادة الحافظة الموجودة في العينة)، ومن ثم يجري الزرع من تلك التمديدات بفرش 0.1 مل على سطح وسط TSA أو وسط SDA موجود في علبة بتري (محضر وجاف بحيث يمتص الماء المرافق للعينة). ثم حضنت العينات بالدرجة 37 مْ لمدة 48 ساعة بالنسبة لكل من الجراثيم وفطر المبيضات البيض، في حين حضنت عينات الرشاشيات السوداء بالدرجة 25 مْ لمدة 7 أيام، وبعد ذلك جرت عملية عد المستعمرات المتشكلة وحساب عدد الجراثيم الحية في 1 مل من المستحضر المختبر.
|
| النتائجResults |
من المعلوم أن هنالك مجموعة من الجراثيم ممنوع وجودها في الأشكال الصيدلانية المأخوذة فموياً، لذلك هدف بحثنا إلى اختبار قدرة نظام الحفظ في أنواع مختلفة من الأشكال الصيدلانية، المنتجة محلياً والمطروحة للاستعمال في الصيدليات في سورية، ضد التلوث بتلك الجراثيم وكانت النتائج على الشكل التالي:
أولاً- الإِشْريكِيَّةُ القولونِيَّة E. coli:
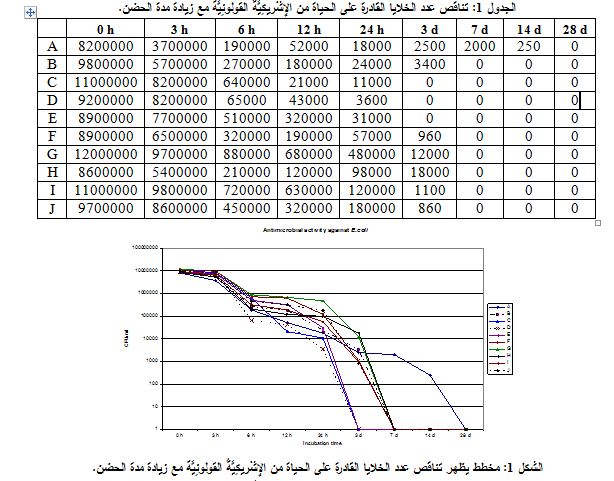
يبين الجدول 1 وكذلك الشكل 1 علاقة عدد الخلايا القادرة على الحياة بالنسبة للإِشْريكِيَّةُ القولونِيَّة الموجودة ضمن المستحضرات المختلفة مع تقدم زمن الحضن، ونلاحظ كما هو واضح في المخطط البياني للشكل 1 أن هنالك تناقصاً في عدد الخلايا القادرة على الحياة ضمن المستحضرات المختلفة بشكل كبير خلال الفترة الأولى من الحضن، حيث يصل العدد الى الصفر (عدم نمو) في اليوم السابع في الشرابات السائلة كلها، بينما استمر عدد قليل من الخلايا (250 خلية/ مل) قادر على الحياة في الشراب المستعلق A.
ثانياً- الكلِبْسيلَّة الرئوية:
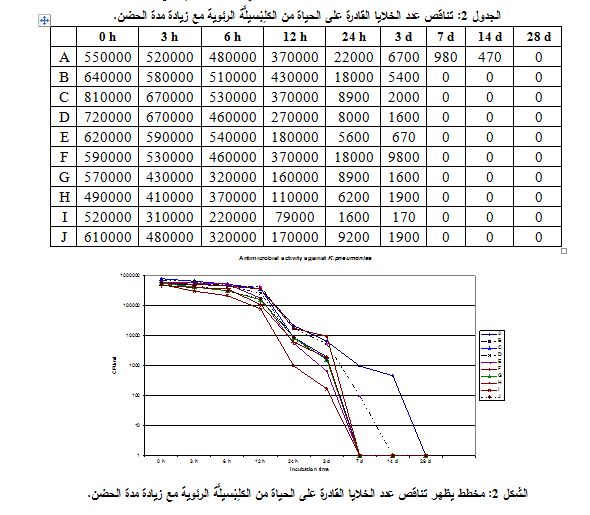
نلاحظ من الجدول 2 والشكل 2 أن عدد خلايا جراثيم الكلِبْسيلَّة الرئوية القادرة على الحياة الموجودة ضمن المستحضرات المختلفة تناقص مع تقدم زمن الحضن، ولكن هنالك تأخر في استجابة الجرثوم لتأثير نظام الحفظ، حيث لم تبدأ عملية التناقص اللوغارتمي إلا بعد مضي 24 ساعة، وكما في حالة للإِشْريكِيَّةُ القولونِيَّة وصل عدد الخلايا القادرة على الحياة في اليوم السابع من الحضن إلى الصفر في المستحضرات جميعها، ما عدا الشراب المستعلق A حيث استمر وجود حوالي 470 خلية/ مل إلى اليوم الرابع عشر من الحضن.
ثالثاً- الزائفة الزنجارية:
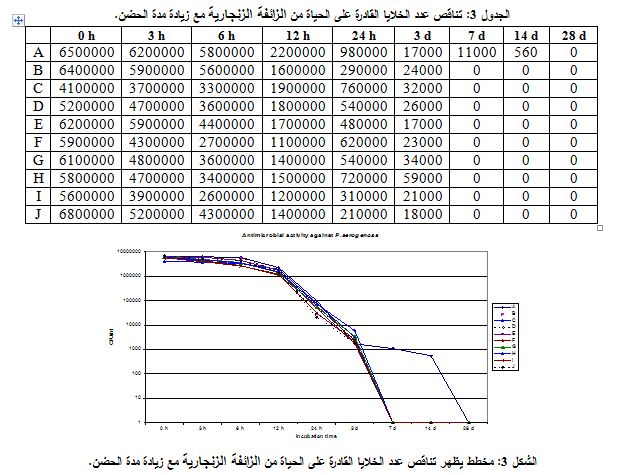
إن جراثيم الزائفة الزنجارية مقاومة للتأثير المضاد للجراثيم للعديد من المضادات الجرثومية المختلفة وهذا ما نلحظه من الجدول 3 والشكل 3، حيث تظهر استجابة هذه الجراثيم لنظام الحفظ في المستحضرات المستعملة مع تقدم زمن الحضن، وكما كان الحال مع الكلِبْسيلَّة الرئوية، نلاحظ أن الزائفة الزنجارية تأخرت كذلك في الاستجابة للقدرة القاتلة لنظام الحفظ لمدة 24 ساعة للمستحضرات المفحوصة جميعها، إلا أنه في النهاية وصل عدد الجراثيم إلى الصفر بعد 7 أيام من الحضن في المستحضرات كلها، إلا في حالات الشراب المستعلق A، حيث بقي عدد من الجراثيم 560 خلية/ مل بعد مضي 14 يوماً.
رابعاً- العنقودية الذهبية:
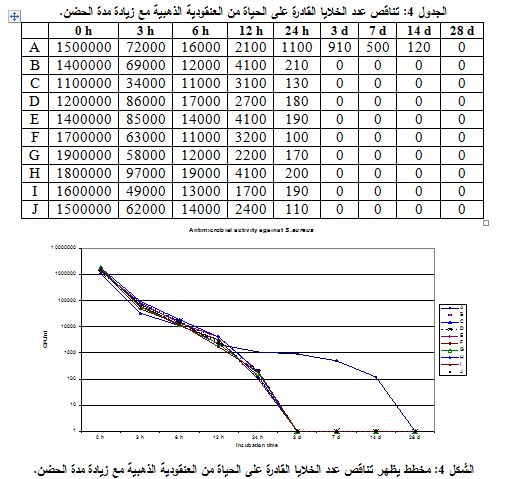
لم تبد العنقوديات مقاومة للقتل بفعل نظام الحفظ ضمن الأشكال الصيدلانية المستعملة، حيث لوحظ التناقص في عدد الخلايا القادرة على الحياة منذ الساعات الأولى للحضن، كما هو موضح في الجدول 4 والشكل 4. حيث أن التناقص اللوغارتمي بدأ سريعاً خلال الساعات الأولى للحضن، وكما في حالة باقي الجراثيم وصل عدد الجراثيم إلى الصفر خلال الأيام السبعة الأولى للحضن للمستحضرات جميعها، وبقي في الشراب المستعلق A عدد قليل من الجراثيم (120 خلية /مل) لليوم الرابع عشر من الحضن.
خامساً- المبيضات البيض:
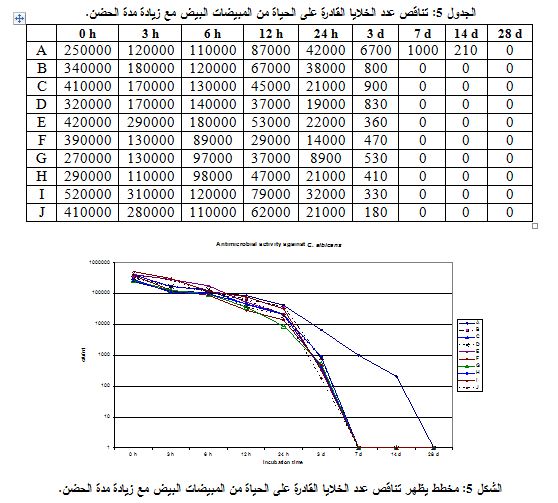
يبين الجدول 5 وكذلك الشكل 5 أن عدد الخلايا القادرة على الحياة من المبيضات البيض بدأ بالتناقص مع زيادة زمن الحضن، حيث لوحظ أن التناقص كان طردياً، وفي معظم الأشكال الصيدلانية المستخدمة في الاختبار وصل العدد
إلى الصفر، أي عدم نمو أي فطر في العينات المأخوذة إلا في حالة الشراب المستعلق A الذي استمر فيه عدد الخلايا الفطرية القادرة على الحياة لمدة 14 يوماً من الحضن.
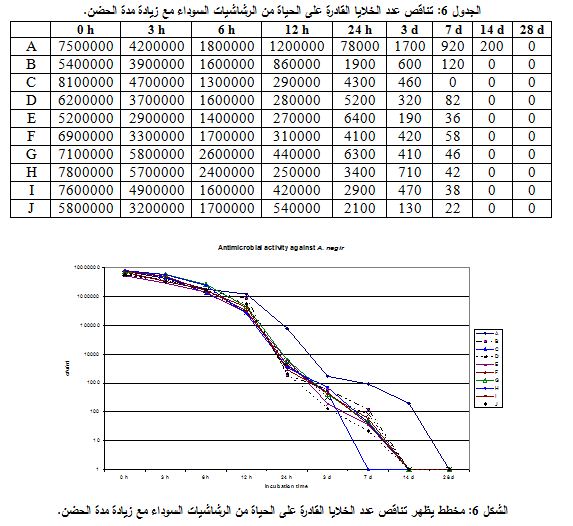
سادساً- الرشاشيات السوداء:
كما هو مبين في الجدول 6 والشكل 6 نلاحظ أن الرشاشيات السوداء، وهي من الفطور الخيطية المتحملة لنسب قليلة من الرطوبة ضمن الشكل الصيدلاني، لم تستطع مقاومة التأثير القاتل لنظام الحفظ، حيث أن النقص في عدد الخلايا القادرة على الحياة مع تقدم زمن الحضن بدا واضحاً بعد 12 ساعة من الحضن، واستمر كذلك حتى اليوم السابع، حيث أن الشراب السائل C فقط وصل فيه عدد الجراثيم إلى الصفر، بينما حصلت هذه النتيجة مع باقي المستحضرات في اليوم الرابع عشر للحضن، وبقي هنالك عدد من الخلايا الفطرية (200 خلية/ مل) في الشراب المستعلق A بعد انقضاء مدة 14 يوماً من الحضن. |
|
| النتائج والمناقشة |
حسب دستور الأدوية الأمريكي 30 (9): لكي يكون نظام الحفظ فعالاً بالنسبة للاختبارات التي تستخدم الجراثيم، يجب أن يحصل نقص ليس أقل من 90% من عدد الجراثيم البدئي (عند الزمن صفر)، بعد 7 أيام من الحضن، وليس أقل من 99% نقص من العدد البدئي (عند الزمن الصفر) بعد 14 يوم حضن، وأن لا يزداد العدد بعد حضن 28 يوماً. أما في حالة الفطور (خمائر وعفونات): يجب أن لا يزداد العدد البدئي (عند الزمن صفر) بعد 7، 14، 28 يوم حضن.
وفقا للمقياس السابق نلاحظ أن المستحضرات المستخدمة في الاختبار كلها كانت موافقة لمتطلب دستور الأدوية الأمريكي، من حيث قدرة نظام الحفظ على منع تخرب الشكل الصيدلاني خلال مدة التخزين والاستخدام.
لوحظ أن الشراب المستعلق A هو الوحيد الذي استمر فيه عدد قليل من الخلايا الجرثومية أو الفطرية القادرة على الحياة بعد مضي 14 يوماً على فترة الحضن. إن سبب ذلك هو طبيعة الشكل الصيدلاني، حيث أن المستحضر هو شراب مستعلق مضاد للحموضة ودرجة الـ pH فيه قلوية (ملائمة لنمو الجراثيم)، كما أن وجود العوالق الصلبة من أملاح الألمنيوم والمغنيزيوم فيه يؤدي إلى ادمصاص كمية كبيرة من المادة الحافظة وبالتالي تقليل الجزء الحر منها (الجزء الفعال) في الوسط المائي وبالتالي إضعاف قدرة نظام الحفظ فيها (10). ومما يؤكد ذلك هو أن دستور الأدوية الأمريكي يكتفي لقياس الـ Antimicrobial effectiveness لهذه المستحضرات بحجم زرعة بدئي (لقاحة Inoculum) فقط 103-104 cfu/ml من الشراب (9). أما أن المستحضرات الأخرى جميعها حصل فيها قتل لكل الخلايا الجرثومية والفطرية المزروعة فيها بعد 14 يوماً من الحضن، ربما يعود ذلك إلى تآزر كل من فاعلية المادة الحافظة مع درجة الـ pH في بعض المستحضرات، ومع نسبة الرطوبة المنخفضة Wa لبعض الأشكال الأخرى.
لوحظ بعض التوافق مع نتائج دراسات عالمية رغم اختلاف عدد الجراثيم المزروعة ونوعها ومدة الحضن (3، 4).
|
| كلمة شكر Acknowledgement |
| جرى هذا العمل في مختبرات كلية الصيدلة في الجامعة الدولية الخاصة للعلوم والتكنولوجيا وبرعاية سامية من قبل المغفور لها بإذنه تعالى الفقيدة الأستاذة الدكتورة غادة الأخرس عميدة الكلية تغمدها الله بواسع رحمته وجعل مثواها الجنة. |
| المراجع References |
1-Fahimdokht Mokhtari
Developing a Test Method for Determining the Effectiveness of Antimicrobial Preservatives.
Research Journal Sciences, 3(9): 984-988, 2008.
2-James Swarbrick
Encyclopedia of Pharmaceutical Technology.
Informa Healthcare, 3rd Edition, 2226, 2007.
3-Khalil R; Khanfar M; Abu Halaweh M; Yacoub M. and Bustami M.
Assessment of the preserving efficacy of the pharmaceutical syrups to identified air-borne microorganisms.
Trends Applied Sci. Res; 6, 198-203, 2011.
4-Khanfar M; Khalil R. and AbuJafal A.
Evaluation of preserving efficacy for different cough syrups manufactured by different pharmaceutical companies.
Int. J. Pharmacol. 5: 319-322. 2009
5-Lucia Clontz
Microbial Limit and Bioburden Tests,
CRC Press-2nd edition, 35-36, 2009.
6-Luis Jimenez
Microbial Contamination Control in the Pharmaceutical Industry.
Marcel Dekker, Inc; 17-38, 2004.
7-Steinberg D.C.
Preservatives as active ingredients.
In: Preservatives for cosmetics, C and T Ingredient resource series, 4-5: 23-24, 1996.
8-Sarfaraz K. Niazi
Hand Book of Pharmaceuticals Manufacturing Formulations.
CRC Press LLC, 2004.
9-USP 31. The United States Pharmacopeia. The United States Pharmacopeial Convention, 2008.
10-Huge W.B. and Russell A.D.
Pharmaceutical Microbiology. Blackwell Scince LTD, 7th edition K, 285-305, 2004.
|
| |
| المجلد 6 ,
العدد 5
, جمادى الأولى 1433 - نيسان (أبريل) 2012 |
|
|
|
